КЧТі> ЦРҝј> ЦРҝј»ҜС§> »ҜС§ДЈДвМв> ОДХВДЪИЭ
2020ДкјӘБЦЦРҝј»ҜС§Б·П°ЈЁ7Ј©
АҙФҙ :ЦР»ӘҝјКФНш 2019-11-29
ЦРЎЎЎЎЛДЎўјЖЛг
ЎЎЎЎ1. ФЪТ»ЙХұӯЦРКўУР22.3g Na2CO3әНNa ClЧйіЙөД№ММе»мәПОпЈ¬јУЧгБҝЛ®ИЬҪвЈ¬ЦЖіЙИЬТәЎЈПтЖдЦРЦрҪҘөОјУИЬЦКЦКБҝ·ЦКэОӘ10%өДПЎСОЛбЈ¬·ЕіцЖшМеөДЧЬЦКБҝУлЛщөОИлПЎСОЛбөДЦКБҝ№ШПөЗъПЯИзНјЛщКҫЈә
ЎЎЎЎЗлёщҫЭМвТв»ШҙрОКМвЈә
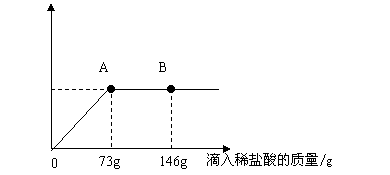
ЎЎЎЎ(1)өұөОјУБЛ73gПЎСОЛбКұЈ¬·ЕіцЖшМеөДЧЬЦКБҝОӘЎЎЎЎЎЎЎЎ gЎЈ
ЎЎЎЎ(2)өұөОјУПЎСОЛбЦБНјЦРBөгКұЈ¬ЙХұӯЦРИЬТәАпөДИЬЦККЗ(Рҙ»ҜС§КҪ)ЎЎЎЎЎЎЎЎЎЎЎЎ ЎЈ
ЎЎЎЎ(3)өұөОјУБЛ73gПЎСОЛбКұ(јҙAөгКұ)Ј¬ЙХұӯЦРОӘІ»ұҘәНИЬТәЈ¬КФНЁ№эјЖЛгЗуіцЖдЦРә¬ИЬЦКөДЦКБҝЎЈ
ЎЎЎЎҙр°ёЈә(№І6·Ц) (1)4.4 (1·Ц)
ЎЎЎЎ(2)NaCl ЎўHClЎЎ(2·ЦЈ¬ҙр¶ФТ»ёцёш1·ЦЈ¬УРҙнПоІ»ёш·Ц)
ЎЎЎЎ(3)(№І3·Ц)ҪвЈә73g10%өДПЎСОЛбЦРә¬HClөДЦКБҝКЗЈә
ЎЎЎЎ73gЎБ10%=7.3gЎЎ(0.5·Ц)
ЎЎЎЎЙиІОјУ·ҙУҰөДМјЛбДЖөДЦКБҝОӘxЈ¬·ҙУҰЙъіЙөДВИ»ҜДЖөДЦКБҝОӘy
ЎЎЎЎNa2CO3 + 2HCl = 2NaCl + CO2Ўь + H2OЎЎ(1·Ц)
ЎЎЎЎ106ЎЎЎЎЎЎ73ЎЎЎЎ117
ЎЎЎЎXЎЎЎЎ 7.3gЎЎЎЎy
ЎЎЎЎЎЎЎЎЎЎЎЎ y=11.7gЎЎ(0.5·Ц)
ЎЎЎЎЙХұӯАпІ»ұҘәНИЬТәЦРИЬЦКөДЦКБҝОӘЈә 117.g + (22.3g-10.6g) = 23.4g (0.5·Ц)ҙрЈәВФ
ЎЎЎЎ2.ҝОНв»о¶ҜРЎЧйОӘІв¶ЁДіұдЦКЗвСх»ҜДЖ№ММеЦРЗвСх»ҜДЖөДЦКБҝ·ЦКэЈ¬ЙијЖЎўҪшРРБЛПВГжөДКөСйЈә
ЎЎЎЎІҪЦиТ»ЈәИЎ5gСщЖ··ЕИл50mLРЎЙХұӯЦРЈ¬јУЧгБҝөДХфБуЛ®ЦБСщЖ·НкИ«ИЬҪв;
ЎЎЎЎІҪЦи¶юЈәПтЙХұӯЦРөОјУВИ»ҜұөКФјБЦБІ»ФЩІъЙъіБөнОӘЦ№Ј¬№эВЛ»мәПОп;
ЎЎЎЎІҪЦиИэЈәҪ«ВЛөГөДіБөнёЙФпЈ¬іЖөГЦКБҝОӘ1.97g
ЎЎЎЎЗлёщҫЭКөСй»ШҙрПВГжОКМвЈә
ЎЎЎЎўЕУРН¬С§ИПОӘТІҝЙТФПтСщЖ·ЦРјУИлПЎСОЛбөД·Ҫ·ЁІв¶ЁЗвСх»ҜДЖөДЦКБҝ·ЦКэЈ¬ЗлДгМёМё¶ФХвёц·Ҫ°ёөДҝҙ·ЁЎЈ
ЎЎЎЎўЖёщҫЭҝОНвРЛИӨРЎЧйІв¶ЁөДКэҫЭјЖЛг№ММеЦРЗвСх»ҜДЖөДЦКБҝ·ЦКэ?(ҫ«И·өҪ0.1%)
ЎЎЎЎҙр°ёЈәўЕјУИлөДСОЛбГ»УРИ«ІҝУГУЪёъМјЛбДЖ·ҙУҰЈ¬Ів¶ЁКұЛщУГСОЛбөДБҝЖ«¶аЎЈБнНвЈ¬·ҙУҰЦРЙъіЙөД¶юСх»ҜМј»№РиЖдЛы·ҙУҰАҙОьКХЈ¬ФміЙјЖЛгЎўІЩЧч№эіМ·ұЛц (1·Ц)
ЎЎЎЎўЖҪвЈәЙиФӯ»мәПОпЦРМјЛбДЖөДЦКБҝОӘx
ЎЎЎЎNa2CO3+BaCl2=2NaCl+BaCO3ЎьЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ (1·Ц)
ЎЎЎЎ106ЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ 197
ЎЎЎЎxЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ 1.97g
ЎЎЎЎ![]() =
=![]()
ЎЎ x=1.06gЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎЎ(1·Ц)
ЎЎЎЎТСұдЦК№ММеЦРЗвСх»ҜДЖөДЦКБҝ·ЦКэ=![]() ЎБ100%=78.8%ЎЎЎЎЎЎ(1·Ц)
ЎБ100%=78.8%ЎЎЎЎЎЎ(1·Ц)
ЎЎЎЎҙрЈә№ММеЦРЗвСх»ҜДЖөДЦКБҝ·ЦКэОӘ78.8%
ДъҝЙДЬёРРЛИӨөДОДХВ
-
2019ДкЦРҝј»ҜС§ТЧҙнСЎФсМвЧЁПоСөБ·
2019-02-13
-
іЙ¶јКР2018-2019ДкіхИэЖЪД©»ҜС§КФМвј°ҙр°ё
2019-01-21
-
јГДПКР2018-2019ДкіхИэ»ҜС§ЖЪД©КФМв
2019-01-18
-
әУДП2018-2019С§ДкіхИэЙПС§ЖЪЖЪД©ҝјКФ»ҜС§КФҫнј°ҙр°ё
2019-01-11
-
2018-2019ДкПеСфҫЕДкј¶»ҜС§ЖЪД©ІвКФМвј°ҙр°ё
2019-01-10
-
2018-2019С§ДкөЪТ»С§ЖЪЖЪЦРҝјКФ»ҜС§КФҫн
2018-11-20

