Ή“≥> ÷–ΩΦ> ÷–ΩΦΜ·―ß> Μ·―ßΡΘΡβΧβ> ΈΡ’¬ΡΎ»ί
2020ΡξΧλΫρ÷–ΩΦΡΘΡβ ‘ΧβΦΑ¥πΑΗΘ®10Θ©
ά¥‘¥ :÷–ΜΣΩΦ ‘Άχ 2019-12-19
÷–ΓΓΓΓ»ΐΓΔ(±Ψ¥σΧβΙ≤5Χβ)
ΓΓΓΓ16. ¥”CaΓΔCΓΔSΓΔHΓΔOΓΔNΝυ÷÷‘ΣΥΊ÷–―Γ‘ώ Β±ΒΡ‘ΣΥΊΑ¥“Σ«σΧνΩ’ΓΘ
ΓΓΓΓ(1)”Ο Β±ΒΡ ΐΉ÷ΚΆΖϊΚ≈ΧνΩ’ΘΚ
ΓΓΓΓΔΌΕΰΗω«β‘≠Ή”______;ΔΎ»ΐΗωΝρΥαΗυάκΉ”______;Δέ“Μ―θΜ·ΒΣ÷–ΒΣœ‘+2Φέ______;
ΓΓΓΓ(2)–¥≥ωΖϊΚœœ¬Ν–“Σ«σΒΡΈο÷ ΒΡΜ·―ß ΫΘΚ
ΓΓΓΓΔΌΉν≥Θ”ΟΒΡ»ήΦΝ_________;ΔΎ≥δ»κ ≥ΤΖΑϋΉΑ¥ϋ÷–Ω…ΖάΗ·ΒΡΒΞ÷ _________;

ΓΓΓΓΔέ≥Θ”Οά¥ΗΡΝΦΥα–‘ΆΝ»άΒΡΦνΓΓΓΓΓΓΓΓΓΓ ;ΔήΡή–Έ≥…ΝρΥα–ΆΥα”ξΒΡΩ’ΤχΈέ»ΨΈο___ΓΘ
ΓΓΓΓ17.(1)Ρ≥‘ΣΥΊΒΡ‘≠Ή”ΫαΙΙ Ψ“βΆΦΈΣΓΓΓΓΓΓΓΓ Θ§ΗΟ‘ΣΥΊ‘≠Ή”ΚΥΡΎ”–______Ηω÷ Ή”Θ§
ΓΓΓΓΉνΆβΒγΉ”≤ψ…œ”–_____ΗωΒγΉ”ΓΘ(2)”ΟΖϊΚ≈±μ ΨΘΚ2Ηω«βΤχΖ÷Ή”_____;1Ηω«β―θΗυάκΉ”_____ΓΘ
ΓΓΓΓ(3)ΉνΫϋΘ§ΩΤ―ßΦ“―–ΨΩΖΔœ÷Θ§Ρ≥–© ≥ΤΖ÷– Ι”ΟΒΡΥ’ΒΛΚλIΚ≈Ω…Ρή÷¬Α©ΓΘΥ’ΒΛΚλIΚ≈ΒΡΜ·―ß ΫΈΣC16H12N2OΘ§ΥϋΒΡ“ΜΗωΖ÷Ή”÷–Ι≤Κ§”–__________Ηω‘≠Ή”Θ§Υϋ «”…__________÷÷‘ΣΥΊΉι≥…ΒΡΘ§Τδ÷–ΒΣΓΔ―θ‘ΣΥΊΒΡ÷ ΝΩ±»ΈΣ__________ΓΘ
ΓΓΓΓ18. ΜπΦΐΆΤΫχΤς÷– Δ”–“ΚΧ§Έο÷ XΚΆΥΪ―θΥ°Θ§Β±ΥϋΟ«ΜλΚœΖ¥”Π ±Θ§Ζ≈≥ω¥σΝΩΒΡ»»Θ§≤ζ…ζ«Ω¥σΆΤΕ·ΝΠΘ§”–ΙΊΒΡΜ·―ßΖ¥”ΠΈΣΘΚX+2H2O2===N2Γϋ+4H2OΘ§‘ρXΒΡΜ·―ß ΫΈΣΓΓΓΓΓΓΓΓΓΘ
ΓΓΓΓ19. œ¬Οφ «Ρ≥Ά§―ßΕ‘ΧζΒΡ–‘÷ ΒΡ―ßœΑΙΐ≥ΧΘΚ
ΓΓΓΓ(1)Ε‘Χζ÷ΤΤΖ…ζ–βΒΡ«ιΩωΒς≤ιΘΚ
|
Βς≤ιΡΎ»ί |
ΒτΤαΒΡΉ‘––≥Β |
¬ψ¬Ε‘ΎΜλΡΐΆΝ “‘ΆβΒΡΗ÷Ϋν |
ΆΩ”ΆΒΡ Έό–βΧζΕΛ |
ΕΤΗθΒΡΧζ÷ ΦτΒΕ |
|
Χζ÷ΤΤΖ–β ¥ ΒΡ«ιΩω |
Ζγ¥Β”ξΝήΘ§ ±Φδ≥ΛΝΥΘ§ΒτΤαΒΡ≤ΩΖ÷Μα…ζ–β |
±Φδ≥ΛΝΥΗ÷Ϋν±μΟφ≥ωœ÷–β≤ψ |
ΧζΕΛΫœ≥Λ ±Φδ »‘≤Μ…ζ–β |
ΦτΒΕΫœ≥Λ ±Φδ ≤Μ…ζ–β |
ΓΓΓΓ¥”Βς≤ι÷–Ω…÷ΣΧζ÷ΤΤΖ…ζ–βΒΡ÷ς“ΣΧθΦΰ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΓΓΓΓ(2)Ά®ΙΐΧζ”κΝρΥαΆ≠»ή“ΚΖ¥”ΠΒΡ Β―ιΘ§ά¥±»ΫœΧζΚΆΆ≠ΒΡΫπ τΜνΕ·–‘«Ω»θΓΘ«κ–¥≥ωΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ_________ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓ20. ≥ΤΖ±Θœ Ω…“‘Ζά÷Ι ≥ΤΖΗ·ΜΒΘ§±Θ≥÷ ≥ΤΖΒΡ”Σ―χΚΆΈΕΒάΓΘ ≥ΤΖ±Θœ ΒΡ¥κ ©”–ΧμΦ”ΖάΗ·ΦΝΓΔ≥δΧνΤχΧεΓΔΖ≈÷ΟΗ…‘οΦΝΚΆΆ――θ±Θœ ΦΝΒ»ΓΘ
ΓΓΓΓ(1)ΑϋΉΑ λ ≥÷ΤΤΖ≥ΘΦ”»κΖάΗ·ΦΝΓΘ±ϊΥαΡΤ «“Μ÷÷ ≥ΤΖΖάΗ·ΦΝΘ§Μ·―ß ΫΈΣC3H5O2NaΘ§±ϊΥαΡΤ «”…_______÷÷‘ΣΥΊΉι≥…Θ§ΤδœύΕ‘Ζ÷Ή”÷ ΝΩΈΣ________;
ΓΓΓΓ(2)–ΓΑϋΉΑΗβΒψάύ ≥ΤΖ≥Θ≤…”Ο≥δΤχΑϋΉΑΘ§ΒΣΤχ «≥Θ”ΟΒΡ≥δΧνΤχΧεΓΘ«κΡψΗυΨίΒΣΤχΒΡ–‘÷ –¥≥ω―Γ”ΟΒΣΤχΒΡ÷ς“Σ‘≠“ρ «___________;
ΓΓΓΓ(3)…ζ ·Μ“ΚΆΙηΫΚ(÷ς“Σ≥…Ζ÷ «Εΰ―θΜ·Ιη) «≥Θ”ΟΒΡΗ…‘οΦΝΓΘ…ζ ·Μ“ΚΆΕΰ―θΜ·ΙηΕΦ τ”Ύ___________(Χν–ρΚ≈);ΓΓΔΌΥαΓΓΓΓΔΎΦνΓΓΓΓΓΓ ΓΓΔέ―ΈΓΓΓΓΓΓΔή―θΜ·Έο
ΓΓΓΓ(4)Ρ≥Ά――θ±Θœ ΦΝ÷ς“Σ≥…Ζ÷ΈΣΜν–‘ΧζΖέΘ§άϊ”ΟΧζ”κ―θΤχΓΔΥ°Ζ¥”Π…ζ≥…«β―θΜ·ΧζΘ§ά¥Έϋ ’ΑϋΉΑ¥ϋ÷–ΒΡ―θΤχΘ§¥”Εχ―”≥Λ ≥ΤΖΒΡ±Θ÷ ΤΎΓΘΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ__________ΓΘ“―÷ΣΗΟΆ――θ±Θœ ΦΝ÷–Μν–‘ΧζΖέΒΡ÷ ΝΩΈΣ1.4gΘ§ΦΤΥψΗΟΆ――θ±Θœ ΦΝΉνΕύΡήΙΜΈϋ ’―θΤχ_______gΓΘ
ΓΓΓΓΥΡΓΔ(±Ψ¥σΧβΙ≤3Χβ)
ΓΓΓΓ21. “ΜΡξΒΡΜ·―ß―ßœΑΘ§Έ“Ο«Ϋ”¥ΞΝΥ≤Μ…ΌΜ·―ßΖ¥”ΠΘ§ΒΪΆ®ΙΐΙιΡ…’ϊάμΘ§ΤδΜυ±ΨΖ¥”Πάύ–ΆΨΆΥΡ÷÷Θ§«κΑ¥œ¬Ν–Ζ¥”Πάύ–Ά–¥≥ωΡψ λœΛΒΡΜ·―ßΖΫ≥Χ Ϋ(ΗςΨΌ“Μάΐ)ΓΘ
ΓΓΓΓ(1)Μ·ΚœΖ¥”Π_______________________;(2)Ζ÷ΫβΖ¥”Π_________________________;
ΓΓΓΓ(3)÷ΟΜΜΖ¥”Π_______________________;(4)Η¥Ζ÷ΫβΖ¥”Π______________________ΓΘ
ΓΓΓΓ22.ΓΓAΓΔBΓΔCΓΔDΥΡΗω…’±≠Ζ÷±π Δ”–50gΥ°Θ§‘ΎœύΆ§ΒΡΈ¬Ε»œ¬Θ§œρΥΡΗω…’±≠÷–“ά¥ΈΦ”»κ27gΓΔ9gΓΔ36gΓΔ18gΒΡΆ§÷÷Έο÷ Θ§≥δΖ÷»ήΫβΚσΒΡ«ιΩω»γΆΦΥυ ΨΘ§Ψ≠Ιέ≤λΚσΜΊ¥πœ¬Ν–Έ ΧβΘΚ
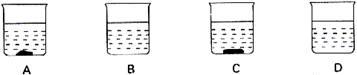
ΓΓΓΓ(1)___________÷– Δ”–ΒΡ“ΜΕ® «≤Μ±ΞΚΆ»ή“ΚΓΘ
ΓΓΓΓ(2)±Θ≥÷Έ¬Ε»≤Μ±δΘ§»γΙϊΫΪAΓΔB…’±≠÷–ΒΡΈο÷ ΜλΚœΚσΘ§»ή“ΚΗ’ΚΟ¥οΒΫ±ΞΚΆΘ§‘ρΗΟΈο÷ ΒΡ±ΞΚΆ»ή“Κ÷–»ή÷ ΒΡ÷ ΝΩΖ÷ ΐ «___________ΓΘ
ΓΓΓΓ23. ”–AΓΔBΓΔC»ΐ÷÷Έο÷ Ης5gΉι≥…ΒΡΜλΚœΈοΘ§‘Ύ“ΜΕ®ΧθΦΰœ¬ΖΔ…ζΜ·―ßΖ¥”ΠΘΚB+C=2A+DΓΘ≥δΖ÷Ζ¥”ΠΚσΒΡ Θ”ύΈο÷ ÷–Κ§”–6g AΓΔ6g DΚΆ»τΗ…ΩΥBΘ§‘ρ≤ΈΦ”Ζ¥”ΠBΓΔCΒΡ÷ ΝΩ±»ΈΣ____ΓΘ
ΓΓΓΓΈεΓΔ(±Ψ¥σΧβΙ≤3Χβ)
ΓΓΓΓ24. Ά§―ßΟ«Θ§Ά®Ιΐ“ΜΡξΒΡ―ßœΑΘ§Ρψ“―’ΤΈ’ΝΥ Β―ι “÷Τ»ΓΤχΧεΒΡ”–ΙΊΙφ¬…Θ§œ¬Οφ«κΡψΫαΚœœ¬Ν–ΉΑ÷ΟΆΦΜΊ¥πΈ ΧβΓΘ(ΖΔ…ζΉΑ÷ΟΚΆ ’Φ·ΉΑ÷ΟΧν–ρΚ≈)
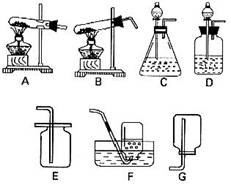
ΓΓΓΓ(1) Β―ι “Ω…”ΟΦ”»»ΗΏΟΧΥαΦΊ÷Τ―θΤχΘ§Ω…―Γ”ΟΒΡΖΔ…ζΉΑ÷Ο «________Θ§ ’Φ·ΉΑ÷Ο «________Θ§ΗΟΤχΧε___________(ΧνΓΑΡήΓ±ΜρΓΑ≤ΜΡήΓ±)»Φ…’;
ΓΓΓΓ(2) Β―ι “÷Τ»ΓΕΰ―θΜ·ΧΦΤχΧε”Π―Γ”ΟΒΡΖΔ…ζΉΑ÷Ο «___________Θ§Ή‘―Γ‘≠ΝœΘ§«κ–¥≥ω“ΜΗωΡή…ζ≥…Εΰ―θΜ·ΧΦΤχΧεΒΡ τ”Ύ÷ΟΜΜΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
ΓΓΓΓ(3)»τ“―÷ΣΡ≥ΤχΧεΩ…―Γ”ΟAΉςΈΣΖΔ…ζΉΑ÷ΟΘ§‘ρ÷Τ»ΓΗΟΤχΧεΒΡΖ¥”ΠΈοΦΑΖ¥”ΠΧθΦΰ”Π¬ζΉψΘΚ______________________Θ§»τΥϋ÷ΜΩ…”Οœρœ¬≈≈Ω’ΤχΖ® ’Φ·Θ§‘ρΗΟΤχΧε”ΠΨΏ±ΗΒΡ–‘÷ «_________________________________ΓΘ
ΓΓΓΓ25 ΆθΟςœκ÷ΤΉς“ΜΗω¥ΔΤχΤΩΘ§ΫΪΦ“÷–ΟΚΤχ¥χΒΫ―ß–ΘΫχ––ΧΫΨΩΓΘ«κΡψΗυΨίœ¬Ν–ΧαΙ©ΒΡ“«ΤςΑο÷ζΥϊ…ηΦΤ“ΜΗω¥ΔΤχΤΩΘ§”Π―Γ”ΟΒΡ“«Τς–ρΚ≈ «_______Θ§“ΣœκΫΪΟΚΤχ¥φ¥ΔΒΫ¥ΔΤχΤΩ÷–Θ§¥ρΩΣΦ–Ή”ΚσΘ§œ»“ΣΫΪ¥ΔΤχΤΩΡΎΉΑ¬ζΥ°Θ§»ΜΚσΓΓ______ ;“ΣœκΫΪ¥ΔΤχΤΩΒΡΟΚΤχ≈≈≥ωΘ§”Πœ»¥ρΩΣΦ–Ή”Θ§»ΜΚσ______ΓΘ

ΓΓΓΓ26 Ζ÷ΩΣ ΔΖ≈ΒΡAΓΔBΝΫ»ή“Κ÷–Θ§Ι≤Κ§”–Na+ΓΔCu2+ΓΔBa2+ΓΔMg2+ΓΔNO3-ΓΔOH-ΓΔSO42-ΤΏ÷÷άκΉ”ΓΘΝΫ»ή“ΚάοΥυΚ§άκΉ”Ης≤ΜœύΆ§Θ§“―÷ΣA»ή“ΚάοΚ§3÷÷―τάκΉ”ΚΆ2÷÷“θάκΉ”Θ§‘ρB»ή“ΚάοΥυΚ§άκΉ””ΠΗΟ «______ΓΘ
ΓΓΓΓΝυΓΔ(±Ψ¥σΧβΙ≤3Χβ)
ΓΓΓΓ27. ΦΉΓΔ““ΝΫΈΜΆ§―ßΖ÷±π”Οœ¬ΆΦΉΑ÷Ο≤βΕ®Ω’Τχ÷–―θΤχΒΡΧεΜΐΖ÷ ΐΘΚ

ΓΓΓΓ(1)ΦΉΆ§―ßΒΡ Β―ι÷–Θ§Β±ΚλΝΉΚΆΡΨΧΩ≥δΖ÷»Φ…’≤Δά以ΒΫ “Έ¬ΚσΘ§¥ρΩΣ÷ΙΥ°Φ–Θ§Ω¥ΒΫΒΡ÷ς“Σœ÷œσ «ΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ;
ΓΓΓΓ(2)““Ά§―ßΒΡ Β―ι÷–Θ§Β±ΚλΝΉΚΆΡΨΧΩ≥δΖ÷»Φ…’≤Δά以ΒΫ “Έ¬ΚσΘ§¥ρΩΣ÷ΙΥ°Φ–Θ§Ω¥ΒΫΒΡ÷ς“Σœ÷œσ «ΘΚ___________________________________;
ΓΓΓΓ(3)»γΙϊΦΉΓΔ““ΝΫΈΜΆ§―ßΩ¥ΒΫΒΡ÷ς“Σœ÷œσ”–Υυ≤ΜΆ§Θ§«κΦρΒΞΫβ ΆΤδ‘≠“ρΘΚ
ΓΓΓΓΦΉ_______________________________;““_______________________________ΓΘ
ΓΓΓΓ28. ”–AΓΔBΓΔCΓΔDΥΡ÷÷Μ·ΚœΈοΘ§A «œθΥα―ΈΘ§B «ΥαΘ§C «ΦνΘ§D «Κ§+3Φέ‘ΣΥΊΒΡ¬»Μ·ΈοΓΘ“‘…œΈο÷ ΦδΖΔ…ζœ¬Ν–Ζ¥”ΠΘΚΔΌAΓΔBΒΡ»ή“ΚœύΜλΘ§≤ζ…ζ≤Μ»ή”ΎœΓœθΥαΒΡΑΉ…Ϊ≥ΝΒμΓΘΓΓΓΓΔΎBΓΔCΒΡ»ή“ΚΆξ»ΪΖ¥”ΠΚσΘ§ΒΟΒΫ ≥―Έ»ή“ΚΓΘΔέCΓΔDΒΡ»ή“ΚœύΜλΘ§≥ωœ÷ΚλΚ÷…Ϊ≥ΝΒμΓΘ ‘ΆΤΕœ–¥≥ωAΓΔBΓΔCΓΔDΒΡΜ·―ß ΫΘΚ
ΓΓΓΓAΘΚ___________;BΘΚ___________;CΘΚ___________;DΘΚ___________ΓΘ
ΓΓΓΓ29. Έß»Τ“ΜΤΩNaOHΙΧΧε «Ζώ±δ÷ ΒΡΈ ΧβΘ§Ά§―ßΟ«’ΙΩΣΧΫΨΩΜνΕ·ΓΘ
ΓΓΓΓ≤ι‘ΡΉ ΝœΘΚNaOH±δ÷ …ζ≥…Na2CO3;Na2CO3»ή“ΚΒΡpH>7ΓΘ
ΓΓΓΓΦΉΆ§―ß”ΟΖ”ΧΣ ‘“ΚΦλ―ι![]() «Ζώ±δ÷ Θ§Ρψ»œΈΣΥϊΡήΖώ≥…ΙΠ___________ Θ§άμ”… «___________ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
«Ζώ±δ÷ Θ§Ρψ»œΈΣΥϊΡήΖώ≥…ΙΠ___________ Θ§άμ”… «___________ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΓΓΓΓ““Ά§―ß»Γ…ΌΝΩΙΧΧε”Ύ ‘Ιή÷–Θ§ΒΈΦ”Ρ≥÷÷ ‘ΦΝΘ§”–¥σΝΩΤχ≈ί≤ζ…ζΘ§”…¥Υ÷ΛΟςNaOH“―Ψ≠±δ÷ ΓΘΡψ»œΈΣΥυΦ” ‘ΦΝΈΣ_________________________________ΓΘ
ΓΓΓΓ±ϊΆ§―ß”ϊ÷ΛΟς±δ÷ ΒΡΙΧΧε÷–…–¥φNaOHΘ§«κΡψΑο÷ζΥϊΆξ≥…“‘œ¬ΧΫΨΩΖΫΑΗΓΘ
|
ΧΫΨΩΡΩΒΡ |
ΧΫΨΩ≤Ϋ÷η |
‘ΛΦΤœ÷œσ |
|
ΡΩΒΡΘΚ ________________________ |
Θ®1Θ©»Γ…ΌΝΩΙΧΧε»ή”ΎΥ°Θ§œρΤδ÷–ΒΈΦ”ΉψΝΩΒΡ___________»ή“Κ |
≤ζ…ζΑΉ…Ϊ≥ΝΒμ |
|
÷ΛΟςΙΧΧε÷–¥φ‘ΎNaOH |
Θ®2Θ©œρΘ®1Θ©ΥυΒΟ»ή“Κ÷–ΒΈΦ”Ζ”ΧΣ ‘“Κ |
Ζ”ΧΣ ‘“Κ±δΚλ |
ΓΓΓΓΤΏΓΔ(±Ψ¥σΧβΙ≤2Χβ)
ΓΓΓΓ30. ≥ύΧζΩσ(÷ς“Σ≥…Ζ÷ «Fe2O3) «“±ΝΕ…ζΧζΒΡ÷ς“Σ‘≠ΝœΓΘ
ΓΓΓΓ»τ≤βΒΟΡ≥≥ύΧζΩσ ·÷–Χζ‘ΣΥΊΒΡ÷ ΝΩΖ÷ ΐΈΣ56%ΓΘ(ΦΌ…η‘”÷ ≤ΜΚ§Χζ‘ΣΥΊ)«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΓΓΓΓ(1)―θΜ·Χζ÷–Χζ‘ΣΥΊ”κ―θ‘ΣΥΊΒΡ÷ ΝΩ±»ΈΣ__________ΓΘ
ΓΓΓΓ(2)ΗΟΩσ ·÷–―θΜ·ΧζΒΡ÷ ΝΩΖ÷ ΐΈΣ__________ΓΘ
ΓΓΓΓ(3)»τ“ΣΒΟΒΫ¥ΩΧζ28tΘ§¥”άμ¬έ…œΦΤΥψ–η“Σ’β÷÷≥ύΧζΩσ ·_______tΓΘ
ΓΓΓΓ31. ΫΪ50g≤Μ¥Ω ≥―Έ―υΤΖ(‘”÷ ≤Μ»ή”ΎΥ°)Ζ≈»κ360gΥ°÷–Θ§≥δΖ÷ΫΝΑηΘ§¥ΐ―υΤΖ÷–ΒΡ¬»Μ·ΡΤ»Ϊ≤Ω»ή”ΎΥ°ΚσΙΐ¬ΥΘ§»Γ¬Υ“Κ117gΘ§œρΤδ÷–Φ”»κΉψΝΩœθΥα“χ»ή“ΚΘ§ΒΟΒΫ28.7gΑΉ…Ϊ≥ΝΒμΘ§ΦΤΥψΘΚ
ΓΓΓΓ(1)ΓΓΓΓΓΓΥυ»Γ117g¬Υ“Κ÷–»ή÷ ΒΡ÷ ΝΩΖ÷ ΐ;ΓΓ(2) ≥―Έ―υΤΖ÷–¬»Μ·ΡΤΒΡ÷ ΝΩΖ÷ ΐΓΘ
ΡζΩ…ΡήΗ––Υ»ΛΒΡΈΡ’¬
-
2019Ρξ÷–ΩΦΜ·―ß“Ή¥μ―Γ‘ώΧβΉ®œν―ΒΝΖ
2019-02-13
-
≥…ΕΦ –2018-2019Ρξ≥θ»ΐΤΎΡ©Μ·―ß ‘ΧβΦΑ¥πΑΗ
2019-01-21
-
ΦΟΡœ –2018-2019Ρξ≥θ»ΐΜ·―ßΤΎΡ© ‘Χβ
2019-01-18
-
Κ”Ρœ2018-2019―ßΡξ≥θ»ΐ…œ―ßΤΎΤΎΡ©ΩΦ ‘Μ·―ß ‘ΨμΦΑ¥πΑΗ
2019-01-11
-
2018-2019Ρξœε―τΨ≈ΡξΦΕΜ·―ßΤΎΡ©≤β ‘ΧβΦΑ¥πΑΗ
2019-01-10
-
2018-2019―ßΡξΒΎ“Μ―ßΤΎΤΎ÷–ΩΦ ‘Μ·―ß ‘Ψμ
2018-11-20

