2020年山东中考化学模拟试题及答案(4)
来源 :中华考试网 2019-12-23
中二、填空题
1. 现有氮气、氢气、氧气、二氧化碳、碳、一氧化碳、碳酸钙、甲烷八种物质,请按要求填写下列空白。(用化学式填写)
(1)约占空气总体积4/5的是________;(2)被称为“零污染燃料”的气体是_______;
(3)其固体易升华,可作致冷剂和用于人工降雨的是________;
(4)有毒性,可燃烧的气体是______;(5)能用于抢救病人,供给呼吸的气体是:______;
(6)在国家西部大开发战略中的“西气东输”的气体主要成分是________;
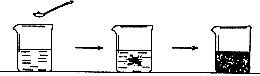
(7)金刚石的成分是________; (8)大理石的主要成分是_________。2. 某学生在研究分子的性质时,做如图所示实验。在一个小烧杯里放半杯水,然后用药匙取一小粒品红,放入烧杯,观察到品红在水中__________。此实验说明分子具有的性质是 。
3. 图A是元素周期表的一部分(图B是相关示例)
|
第二 周期 |
3 Li 锂 7 |
4 Be 铍 9 |
5 B 硼 11 |
① |
7 N 氮 14 |
8 O 氧 16 |
9 F 氟 19 |
10 Ne 氖 20 |
|
第三 周期 |
② |
12 Mg 镁 27 |
13 Al 铝 27 |
14 Si 硅 28 |
③ |
16 S 硫 32 |
17 Cl 氢 35.5 |
19 Ar 氩 40 |
回答下列问题:(1)原子序数为17的元素名称为_______________;
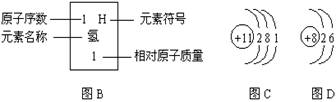
(2)图C是某元素的原子结构示意图,该元素在图A中的位置是(选填①或②或③)_______;(3)图D是氧元素的原子结构示意图,图A中与氧元素在同一纵行的硫元素其原子结构与氧原子相似。由此推测,硫原子在化学反应中易(填“得”或“失”)_______电子。
4. t1℃时,将3g生石灰加入到60g a%的饱和石灰水中,保持温度不变,所得溶液的质量(填“>”、“<”或“=”,下同) _______60g,溶液中溶质的质量分数________a%;若将该溶液的温度升高到t2℃,此时所得溶液中溶质的质量分数_________a%。
5. 除去氯化钠溶液中混有的少量硫酸钠,可选用的除杂试剂是__________ ;除去硫酸亚铁溶液中混有少量硫酸铜,可选用的物质是__________ 。
三、实验题
1. 根据下列实验装置图回答(装置用序号表示):
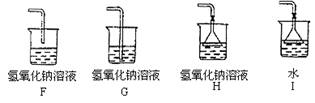
(1)写出编号为①②的仪器名称:①__________,②__________。
(2)实验室制取O2应选用的发生装置是__________;实验室制取CO2应选用的发生装置是__________。
(3)硫化氢是一种有毒的气体,其密度比空气大,能溶于水,它的水溶液叫氢硫酸。实验室通常用块状固体硫化亚铁(FeS)与稀硫酸在常温下反应制取硫化氢气体,制取气体应选用的发生装置是__________,收集装置是__________,气体由__________(填导管口代号)导入集气瓶。(4)收集气体后,对H2S尾气要进行特别处理,以防止污染环境。现有如下装置, 处理H2S尾气的效果最好的装置是________________。
2. 有一包固体粉末,可能由CaCO3、Na2SO4、Na2CO3、CuSO4和BaCl2中的一种或几种组成,做实验得以下结果:
(1)此固体粉末加到水中,得到白色沉淀,上层清液为无色; (2)滴入足量稀硝酸后白色沉淀部分溶解。从实验可判断出,该粉末可能的三组组成:
<1>__________ ;<2> __________ ;<3> __________ 。
3. A、B、C、D四个试剂瓶中分别盛碳酸钠、硝酸银、烧碱、稀硫酸四种稀溶液中的一种,取四种溶液各少量,依次滴入物质X的溶液和稀硝酸,发生的现象如下表所示:
|
A |
B |
C |
D | |
|
X |
白色沉淀 |
白色沉淀 |
白色沉淀 |
无现象 |
|
稀硝酸 |
沉淀不消失 |
沉淀消失,有气体产生 |
沉淀不消失 |
无现象 |
回答:(1)物质X的化学式是_________。
(2)物质B是________,加入X后反应的化学方程式是__________,加稀硝酸后,沉淀消失的反应化学方程式是___________________________。
(3)为进一步区别A和C,可根据置换反应的原理进行实验,写出其中一个反应的化学方程式___________________________。
四、计算题
1. 维生素是人体必备的营养物质,某种维生素D2的化学式为C28H44O,计算:
(1)维生素D2的相对分子质量__________ ;(2)维生素D2中的碳、氢、氧三种元素的质量比__________;(3)198g维生素D2中含碳元素_____________g。
2. 为测定某硝酸银溶液中硝酸银的含量,取20g溶液于烧杯中,加入5.5g盐酸(足量)使溶液中的硝酸银完全反应,将产生的白色沉淀过滤、洗涤、干燥后,称量为2.87g。
(1)求上述20g溶液中AgNO3的质量。
(2)在实验操作中,通常是通过量取液体的体积来取用一定量的液体,查得上述盐酸在实验条件下的密度为1.1 g/mL,则在本实验中所用的5.5g盐酸的体积是多少mL?

