2019�п���ѧģ�����⼰����ģ���1
��Դ :�л������� 2019-05-09
��һ.ѡ����
����1.�����dz��л�ѧ�е�һЩ�������飬���ܴﵽʵ��Ŀ����(����)
����A.
������ȡ����
B.
����ϡ��Ũ����
����C.
�������װ��������
D.
���������
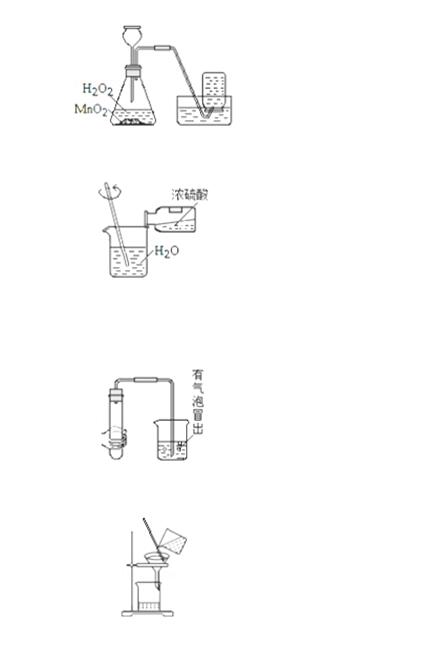
�������㣺��������ȡװ��;Ũ��������ʼ�Ũ�����ϡ��;���˵�ԭ������������Ӧ��;���װ�õ�������;�������ռ�����.
����ר�⣺������������ѧʵ���������.
����������A������ʵ������ȡ������ע��������з����ж�.
����B������Ũ�����ϡ�ͷ���(����ˮ�������ڣ������������Ͻ�)���з����ж�.
����C�����ݼ��װ�������Եķ������з����ж�.
����D������Һ��ʱ��ע�⡰һ�������͡���������ԭ��.
������𣺽⣺A��ʵ�����ù�Һ��������ȡ����ʱ��Ϊ��ֹ�����������ӳ���©�����ݳ�������©����ĩ��Ӧ����Һ�����£�ͼ�г���©����ĩ��û������Һ�����£�ͼ����ʾ��������.
����B��ϡ��Ũ����ʱ��Ҫ��Ũ���Ỻ����������ע��ˮ�У�ͬʱ�ò��������Ͻ��裬��ʹ������ʱ����ɢ;һ�����ܰ�ˮע��Ũ������;ͼ����ʾ������ȷ.
����C�����װ�������Եķ������ѵ��ܵ�һ�˽�û��ˮ�˫�ֽ���������ڣ������ܿ�������ð����װ�ò�©��;ͼ����ʾ������ȷ.
����D������Һ��ʱ��Ҫע�⡰һ�������͡���������ԭ��ͼ����ʾ������ȷ.
������ѡ��A.
���������������ѶȲ�����Ϥ������������;��ʹ��ע�����������ѧʵ�����������ע�������ǽ���������Ĺؼ�.
����2.��ʵ�����ø��������������ʵ���У������������(����)
����A.
�����ձ�
B.
����������
C.
����ʯ����
D.
�����Թ�
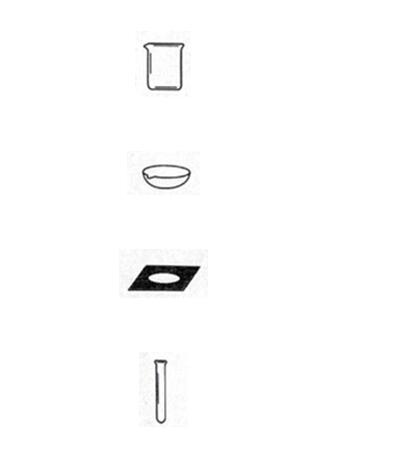
�������㣺��������ȡװ��.
����ר�⣺���������ʵ�����Ʒ������顢�����뾻��.
����������ʵ�����ø��������������װ���У���Ҫʹ�õ������оƾ��ơ�����̨���Թܡ������ܵ���Ƥ��������ƿ��.
������𣺽⣺ʵ�����ø��������������װ���У������������װҩƷ������ص��Թܣ��ձ�����������Һ��ҩƷ���������ʯ�������������������ʲ���Ҫ�ձ���������ʯ����;
������ѡ��D.
�����������˽���������ȡ��������������˳������ձ�����������Һ��ҩƷ���������ʯ����������������.
����3.ʵ���Ҽ��ȸ����������������ֱ�Ӳ��õķ���װ����(����)
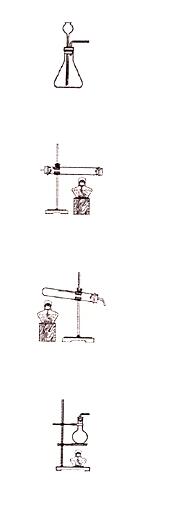
����
�������㣺��������ȡװ��.
����ר�⣺���������ʵ�����Ʒ������顢�����뾻��.
����������A������A���ڹ�Һ�����ͽ��;
����B������B�������ڽ��������ұ�����;
����C�����ݴ��ü��ȸ�����صķ�����ȡ��������Ӧ��Ҫ����;ʵ�����ø��������ȡ����ʱ��������ط�ĩ������������˳�ŵ��ܽ���ˮ�ۣ�ʹˮ���ڵ�ˮ����Ϻ�ɫ(���ڸ����������ˮ���Ϻ�ɫ)��Ϊ��ֹ��������ķ�����ͨ��Ҫ���Թܿڷ�һ����ȥ����;
����D������D����Һ���������.
������𣺽⣺
����A��A���ڹ�Һ������;
����B��B�������ڽ��������ұ��;
����C���ü��ȸ�����صķ�����ȡ������������������ͬʱ����������غͶ����������ɣ����ڷ�Ӧ��Ҫ���ȣ����Է���װ��ӦѡC;ʵ�����ø��������ȡ����ʱ��������ط�ĩ������������˳�ŵ��ܽ���ˮ�ۣ�ʹˮ���ڵ�ˮ����Ϻ�ɫ(���ڸ����������ˮ���Ϻ�ɫ)��Ϊ��ֹ��������ķ�����ͨ��Ҫ���Թܿڷ�һ����;
����D��D����Һ�������װ��.
�����𰸣�C
����������ʵ������ȡ����ʱ������װ�õ�ѡ��ȡ���ڷ�Ӧ���״̬�ͷ�Ӧ����;�ռ�װ�õ�ѡ��ȡ����ˮ���Ժ�������ܶ�;������ʵ������ȡ�����ķ�Ӧԭ������ע������ǿ��Ե��ص�Ҳ���п����ص�.
����4.ʵ���Ҽ��ȸ����������������ֱ�Ӳ��õķ���װ����(����)
�������㣺��������ȡװ��.
����ר�⣺���������ʵ�����Ʒ������顢�����뾻��.
������ʵ�����ø��������ȡ���������ڹ������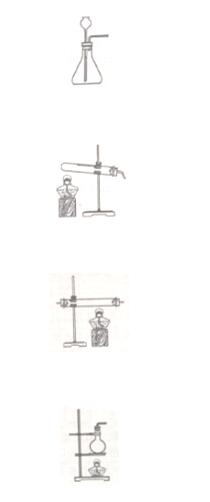 ����ȡ���壬�ݴ˽��з������.
����ȡ���壬�ݴ˽��з������.
������𣺽⣺��������ڼ�����������������ء��������̺����������ڹ����������ȡ����.
����A��ͼ����ʾ��ȡװ��Ϊ��Һ������װ�ã�ʵ���Ҽ��ȸ����������������ѡ�ø�װ�ã���ѡ�����.
����B��ͼ����ʾ��ȡװ��Ϊ���������װ�ã���ѡ����ȷ.
����C��ͼ����ʾ��ȡװ�����˿��ڣ���������ʵ���Ҽ��ȸ����������������ѡ�����.
����D��ͼ����ʾ��ȡװ�ò�������ʵ���Ҽ��ȸ����������������������ˮ��������ȵ���ƿ�ײ���ʹ��ƿ�ײ�ը�ѣ���ѡ�����.
������ѡ��B.
���������������ѶȲ������п�����Ҫ����֮һ����������ʵ��������ȡ������Ӧԭ��������װ�õ�ѡ����������ȷ�����Ĺؼ�.
����5.ʵ��������ͼ��ʾװ����ȡ�����������й�˵������ȷ����(����)
����A.�Թ��м����ҩƷ��MnO2��H2O2
����B.ʵ��ǰӦ���װ�õ�������
����C.�����ܿڲ����������ȵ�����ʱ�ſ�ʼ�ռ�����
����D.ʵ�����ʱӦ�ȴ�ˮ����ȡ�����ܣ���ֹͣ����
�������㣺��������ȡװ��;��ȡ�����IJ��������ע���.
����ר�⣺���������ʵ�����Ʒ������顢�����뾻��.
����������A�����ݸ�װ����ȡ�����ķ�Ӧ���ǹ��壬��Ӧ�����Ǽ��Ƚ��з���;
����B������ʵ��ĵ�һ���Ǽ��װ�õ������Խ��з���;
����C�������ռ���������ȷʱ�̽��з���;
����D�������ռ���ɺ��Ȱѵ����Ƴ�ˮ�棬��Ϩ��ƾ��ƣ����Է�ֹˮ������ը���Թܽ��з���.
������𣺽⣺A����װ����ȡ�����ķ�Ӧ���ǹ��壬��Ӧ�����Ǽ��ȣ���A����;
����B�����װ����������ʵ�������һ����������B��ȷ;
����C����ʼ���������������������������Ҿ���ð��ʱ������������C��ȷ;
����D���ռ���ɺ��Ȱѵ����Ƴ�ˮ�棬��Ϩ��ƾ��ƣ����Է�ֹˮ������ը���Թܣ���D��ȷ.
������ѡ��A.
���������������㿼������������ȡ����������������ռ�������Ҫ��ǿ�����йص�֪ʶ�㣬������Ӧ�ã���������Ҫ������ѡ�����ʵ������.
����6.��ͼ��ʾʵ�������ȷ����(����)

����A.
�����ռ�����B.
��������ҺpHC.
����ȡ��Һ��D.
����ϡ��Ũ����
�������㣺�������ռ�����;Һ��ҩƷ��ȡ��;Ũ��������ʼ�Ũ�����ϡ��;��Һ�����Ȳⶨ.
����ר�⣺������������ѧʵ���������.
����������A�������������ſ������ռ�������ע��������з����ж�.
����B��������pH��ֽ�ⶨδ֪��Һ��pH�ķ������з����ж�.
����C���������Թ����㵹Һ��ҩƷ�ķ������з����ж�.
����D������Ũ�����ϡ�ͷ���(����ˮ�������ڣ������������Ͻ�)���з����ж�.
������𣺽⣺A���������ſ������ռ�����ʱ������Ӧ�쵽����ƿ�ĵײ��������ڿ������ų���ͼ�е���û���쵽����ƿ�ĵײ���ͼ����ʾ��������.
����B����pH��ֽ�ⶨδ֪��Һ��pHʱ����ȷ�IJ�������Ϊ�ò�����պȡ��������Һ���ڸ����pH��ֽ�ϣ������ɫ���Ա���ȷ��pH.���ܽ�pH��ֽ�������Һ�У�������Ⱦ����Һ��ͼ����ʾ��������.
����C�����Թ����㵹Һ��ҩƷʱ��ƿ��Ҫ���ţ���ǩҪ�����ģ�ƿ�ڽ���;ͼ��ƿ��û�н�����ƿ��û�е��š���ǩû���������ģ���ʾ��������.
����D��ϡ��Ũ����ʱ��Ҫ��Ũ���Ỻ����������ע��ˮ�У�ͬʱ�ò��������Ͻ��裬��ʹ������ʱ����ɢ;һ�����ܰ�ˮע��Ũ������;ͼ����ʾ������ȷ.
������ѡ��D.
���������������ѶȲ�����Ϥ������������;��ʹ��ע�����������ѧʵ�����������ע�������ǽ���������Ĺؼ�.
����7.����ͼ���ʵ�������ȷ����(����)
����A.
������������
B.
����ȡ��ҩƷ
C.
������ȡNaCl
D.
����ϡ��Ũ����
�������㣺�����ļ��������;������-������ƽ;����ҩƷ��ȡ��;Ũ��������ʼ�Ũ�����ϡ��.
����ר�⣺������������ѧʵ���������.
����������A������������������ȷ��������;
����B������ҩƷ���и�ʴ�Է���;
����C������������ƽ��ʹ��Ҫ��ѭ���������ԭ��;
����D������ϡ��Ũ�������ȷ��������.
������𣺽⣺A������ʱ��Ӧ�������ǵ�ľ�����ڼ���ƿ�ڣ�ľ����ȼ��˵�������������ʲ�������;
����B��ҩƷ���и�ʴ�ԣ���������ֱ��ȡ�ã��ʲ�������;
����C��������ƽ��ʹ��Ҫ��ѭ���������ԭ�����Ȼ��Ʋ���ֱ�ӷ��������У���������;
����D��ϡ��Ũ����ʱ����Ũ��������ע��ˮ�У������Ͻ��裬�ʲ�����ȷ.
������ѡD.
����������Ҫ��ǿα�����ʵ��Ļ����������������裬��Ҫ����ʵ��ʱ���д������.��������һЩ����ȫ����.
����8.�����й�ʵ���������������������(����)
����A.��ˮ���ռ�O2�������ܿڸ�������ð�������ռ����ռ�����O2������
����B.ȥ�����������������ʣ�������ȫ������ˮ���������ˣ����²���ƫ��
����C.�ⶨ������O2��������ȼ�����������뼯��ƿ������ƿ�������²ⶨ���ƫ��
����D.̽��CO2���ʣ���CO2���ٵ���ʢ��ȼ��������ձ��У����ڹ۲�ʹ�������Ϩ��
�������㣺��ȡ�����IJ��������ע���;������ɵIJⶨ;������̼�Ļ�ѧ����;�Ȼ���������ᴿ.
����ר�⣺������������ѧʵ���������.
����������A�����ݸ�������ð��ʱ���ռ������岻�����;
����B������ȥ�����������������ʣ�������ȫ������ˮ�У��������ˣ�����û��ȫ���ܽ���;
����C���������ڲ���ȼ�ճ�̫����������ƿ��֮ǰ��ƿ�ڲ��ֿ��������ݳ���ʹƿ�ڵ����������֮�������Ҳ�ܵ���ƿ����;
����D������̽��CO2���ʣ���CO2��������ʢ��ȼ��������ձ��н��.
������𣺽⣺
����A�����ܿڸ�������ð�������ռ�����ʱ�ռ��������л��п�������Ӱ�����������ʵ�飬�ʴ���;
����B��ȥ�����������������ʣ�������ȫ������ˮ�У��������ˣ�����û��ȫ���ܽ⣬���²���ƫ�ͣ���ȷ;
����C�����ڲ���ȼ�ճ�̫����������ƿ��֮ǰ��ƿ�ڲ��ֿ��������ݳ���ʹƿ�ڵ����������֮�������Ҳ�ܵ���ƿ�⣬�ᵼ��Һ��ˮ����������;
����D��̽��CO2���ʣ���CO2��������ʢ��ȼ��������ձ��У����ڹ۲�ʹ�������Ϩ�𣬹ʴ���.
�����𰸣�B
����������������Ŀ������ѧ��˼ά�Ŀ����ԣ��ر���֪ʶ��������һ���ļ��ɣ�Ҫ���Լ��а��յ�����.
����9.����ʵ�������ȷ����(����)
����A.��ˮ���ռ�����ʱ�������ܿڿ�ʼ������ð��ʱ�����ռ�
����B.ϡ��Ũ����ʱ�����ձ��ڽ�ˮ����ע��ʢ��Ũ������ձ��У����ò��������Ͻ���
����C.����ʱ���ò������ڹ������в��Ͻ���
����D.����������ȿ�ȼ�������ȼǰ�����鴿
�������㣺��ȡ�����IJ��������ע���;Ũ��������ʼ�Ũ�����ϡ��;���˵�ԭ������������Ӧ��;������һ����̼������ȿ�ȼ������鴿.
����ר�⣺������������ѧʵ���������.
����������A������ʵ������ȡ�����IJ�����з����ж�;
����B������Ũ�����ϡ�ͷ������з����ж�;
����C�����ݹ���ʱ��ע��������;
����D�����ݿ�ȼ������ȼ��ʱ������ը����ȼǰ�����鴿���.
������𣺽⣺
����A����ˮ���ռ�����ʱ������������ð�������ռ�������Ҫ�ȵ�����ð�����Ⱥ����ռ����ʴ���;
����B��Ũ��������ˮҪ���ȣ�����ϡ��Ũ����ʱҪ��Ũ���ᵹ��ˮ�У����ò��������Ͻ��裬�ʴ���;
����C������ʱ���ò����������������ڹ������в��Ͻ��裬��������ֽ���ʴ���;
����D����ȼ������ȼ��ʱ������ը����ȼǰ�����鴿������ȷ.
�����𰸣�D
���������������ѶȲ�����Ϥ������������;��ʹ��ע��������ճ�����ѧʵ�����������ע�������ǽ���������Ĺؼ�.
����10.��һ���������������Ĺ���������Һ���������������̣������д�������������������˵����ȷ����(����)
����A.���������к���ˮ������
����B.����������ʹ�������̷ֽ�ų�����
����C.���������ܼӿ��������ֽ�����ˮ������
����D.�÷�Ӧ���й�������Ͷ����������ַ�Ӧ������ڷֽⷴӦ
�������㣺ʵ������ȡ�����ķ�Ӧԭ��;�������ص��������;��Ӧ���͵��ж�.
����ר�⣺������ˮ.
��������������ʵ���ҷֽ����������ȡ�����ķ�Ӧԭ�������������ڶ������̵Ĵ������·ֽ�����ˮ���������ݴ˽��з������.
������𣺽⣺A�����������в���ˮ����������ѡ��˵������.
����B�����������ڶ������̵Ĵ������·ֽ�����ˮ�����������������ܼӿ��������ֽ�����ˮ����������ѡ��˵������.
����C�����������ڶ������̵Ĵ������·ֽ�����ˮ�����������������ܼӿ��������ֽ�����ˮ����������ѡ��˵����ȷ.
����D���÷�Ӧ�ж�����������������Ӧǰ���������䣬�÷�Ӧ�ķ�Ӧ���ǹ������⣬��������ˮ�����������ϡ�һ��ࡱ�����������ڷֽⷴӦ����ѡ��˵������.
������ѡ��C.
���������������ѶȲ�������ʵ���ҷֽ����������ȡ�����ķ�Ӧԭ��������������ȷ�����Ĺؼ�.
����11.ʵ����������غͶ���������ȡ�������йظ�ʵ���˵���������(����)
����A.���������Ƿ�Ӧ��
����B.����������ȡ����װ����ͬ
����C.���������ſ������ռ�
����D.���ô����ǵ�ľ̿��������
�������㣺ʵ������ȡ�����ķ�Ӧԭ��;�������ռ�����;�����ļ��������.
����ר�⣺���������ʵ�����Ʒ������顢�����뾻��.
��������������������ڶ������̵Ĵ������¼��������Ȼ��غ���������Ϸ�Ӧ���״̬�ͷ�Ӧ������������װ�ã������������ܶȺ��ܽ��Է����ռ�������������������ȼ�Է������鷽��.
������𣺽⣺A��������ڶ������̵Ĵ������¼��������Ȼ��غ����������еĶ���������Ϊ��Ӧ�������Ǵ�������˵������;
����B��������ڶ������̵Ĵ������¼��������Ȼ��غ��������ͼ��ȸ��������ȡ�������ǹ�������͵ķ���װ�ã���˵����ȷ;
����C����Ϊ�������ܶȱȿ�������˿��Բ��������ſ������ռ�����˵����ȷ;
����D������������ȼ�ԣ���˿���ʹ�����ǵ�ľ̿��ȼ����������������˵����ȷ;
������ѡ��Ϊ��A.
�������������⿼��������ȷ���ռ�װ�õ�ѡ�������ļ��鷽����ѡ����װ��ʱ��Ҫ���Ƿ�Ӧ���״̬����Ӧ����������;ѡ���ռ�װ��ʱ��Ҫ���������ˮ���ԡ��ܶȡ��ܷ�Ϳ����е����ʷ�����ѧ��Ӧ�����أ����ڻ����ԵĿ���.
������.�����
����1.��ͼ����������ȡ������ʵ��װ��ͼ.
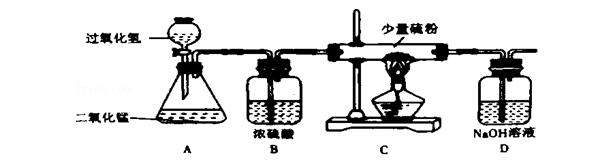
�����ش��������⣺
����(1)װ��B�������ǡ�������������װ��C�����ȼ�յ������ǡ�������������װ��D�������ǡ�����������.
����(2)װ��A�з�����Ӧ�Ļ�ѧ����ʽΪ��������������װ��D�з�����Ӧ�Ļ�ѧ����ʽΪ������������.
�������㣺��������ȡװ��;�����Ļ�ѧ����;�������ռ�����;��д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ.
����ר�⣺���������ʵ�����Ʒ������顢�����뾻��.
����������(1)װ��B��ҩƷ��Ũ���ᣬŨ���������ˮ��;���ȼ�����ɶ����������壬��������������������������Һ��Ӧ�����������ƺ�ˮ���ݴ˽��з������.
����(2)���������ڶ������̵Ĵ�����������ˮ��������д����Ӧ�Ļ�ѧ����ʽ����;
������𣺽⣺(1)װ��B��ҩƷ��Ũ���ᣬŨ���������ˮ�ԣ�װ��B�������dz�ȥˮ����(�������������ˮ��).
����װ��C�����ȼ�յ������������ɫ���棬���ȼ�����ɶ����������壬��������������������������Һ��Ӧ�����������ƺ�ˮ����װ��D�����������ն�������ֹ��Ⱦ����.
����(2)���������ڶ������̵Ĵ�����������ˮ����������Ӧ�Ļ�ѧ����ʽΪ��2H2O2
����2H2O+O2��.
����װ��D�з�����Ӧ�Ļ�ѧ����ʽΪSO2+2NaOH=Na2SO3+H2O.
�����ʴ�Ϊ��(1)��ȥˮ����(�������������ˮ��);��������ɫ����;���ն�������ֹ��Ⱦ����;
����(2)2H2O2
����2H2O+O2��;SO2+2NaOH=Na2SO3+H2O.
���������������ѶȲ������п�����Ҫ����֮һ����������ʵ��������ȡ�����ķ�Ӧԭ���������Ļ�ѧ���ʵ�����ȷ�����Ĺؼ�.
����2��(1)ʵ���Ҹ����ṩ��������������ѡ�ú��ʵ��������ָ����ʵ��.

������ͼ������d�������ǣ�������������.
������Ҫ��ȡ�϶��O2����̽��������(Ҫ����ȡ�����п������ӷ�Ӧ��)����װ���巢��װ����Ҫ�������ǡ�����������(����ţ���ͬ)����д���÷�Ӧ�Ļ�ѧ����ʽ���������������ռ�����Ӧ���á��������������������ռ������Ǹ��������ġ���������������.
�������ᴿ����ʱ��������Ҫѡ�����������еġ�����������(�����)������֮�ȱ�ٵ���������ֽ����������������������������(������).
����(2)Ϊ̽������X����ɣ�ij��ȤС�������ͼ��ʾʵ��(�̶�װ��δ����).
�������������ߡ�
�����ټ��������£�����X��������ͭ��Ӧ����ͭ��ˮ�͵���.
�����ڼ�ʯ��Ϊ�����������ƺ��������ƵĻ�����������X��Ӧ.��ˮ�Ȼ��ƿ���������X.
�����۱�ʵ�������£������ܶ�Ϊ1.15g•L��1��װ���ڿ����е�ˮ�������̼��������ݲⶨ��Ӱ��ɺ��Բ���.��ʵ�鲽�衿
���������������������װ��������.
������ȡһ��������ͭ��ȷ�Ƶ�������Ϊ2.40g.
�����۰�ͼ��ʾװ��ҩƷ(����B��C���зֱ�װ�����������ʯ�Һ�������ˮ�Ȼ���)���Ⲣ��¼�������ݢ�(����).
����������A��B��Cװ�ã�������X����ͨ��һ��ʱ���������Dװ�ã�������ʼ����.��Aװ��������ͭ��Ӧ��ȫ��ֹͣ���ȣ�����ͨ������X����������ȴ���ٴβ�������¼������ݢ�(����).
������ʵ��װ�á�
������������ݡ�
����������Ŀ/���ݱ�Ţ��
����������(��ҩƷ)������/g52.4051.92
����Bװ��(��ҩƷ)������/g102.00102.54
�������������/mL/243.5
�������ش����⡿
������B��װ������������ˮ��ԭ��Ϊ������������(�û�ѧ����ʽ��ʾ).
������ʵ������У����۲쵽��������������˵������ͭ�ѷ�Ӧ��ȫ��ֹͣ���ȣ�����ͨ������X����������ȴ��Ŀ���ǡ�����������.
�����۷���ʵ����������ݣ�����ˮ������Ϊ������������g������ͭ����Ԫ�ص�����Ϊ������������g.�ɴ���֪������X��һ��������������(��С���û�С�)��Ԫ��.
������ͨ�������Ƶ�������X�Ļ�ѧʽΪ������������;����X��ԭ����ͭ�Ļ�ѧ����ʽΪ��������������.
�������㣺��������ȡװ��;ʵ��̽�����ʵ���ɳɷ��Լ�����;���˵�ԭ������������Ӧ��;��������ļ�������ӷ���;�������ռ�����;��д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ.
����ר�⣺���������ʵ�����Ʒ������顢�����뾻��;��ѧ̽��.
��������������©�������Һ��ҩƷ����ȡװ�ð������ȺͲ���������֣������˫��ˮ�Ͷ��������������Ͳ���Ҫ���ȣ�����ø�����ػ����������������Ҫ����.�������ܶȱȿ������ܶȴ�������ˮ��������������ſ���������ˮ���ռ�.�����õ��������У��ձ���©����������������̨.B��װ������������ˮ��ԭ��Ϊ�������ƺ�ˮ��Ӧ������������;ʵ������У����۲쵽��Dװ���������ܵ�Һ�治���½���˵������ͭ�ѷ�Ӧ��ȫ��ֹͣ���ȣ�����ͨ������X����������ȴ��Ŀ���ǣ���ֹ������������ɵ�ͭ������������;����ʵ����������ݣ�����ˮ������=102.54g��102.00g=0.54g;����ͭ����Ԫ�ص�����=52.40g��51.92g=0.48g;�ɴ���֪������X��һ��û����Ԫ�أ���Ϊ0.54gˮ�к���Ԫ��0.48g;ͨ�������Ƶ�������X�ǰ���������������ͭ�ڼ��ȵ�����������ͭ��ˮ�͵�������ƽ����.
������𣺽⣺(1)�ٳ���©�������Һ��ҩƷ���ʴ�Ϊ������©��;
�����������˫��ˮ�Ͷ��������������Ͳ���Ҫ���ȣ�Ҫ����ȡ�����п������ӷ�Ӧ������װ���巢��װ����Ҫ�������ǣ�adf;���������ڶ�������������������������ˮ��������Ҫע����ƽ;�������ܶȱȿ������ܶȴ�������ˮ��������������ſ���������ˮ���ռ�;�ʴ�Ϊ��adf;2H2O2
����2H2O+O2��;�����ſ�����;�ܶȱȿ������ܶȴ�;
�����۹����õ��������У��ձ���©����������������̨;�ʴ�Ϊ��eh;©����������;
����(2)��B��װ������������ˮ��ԭ��Ϊ�������ƺ�ˮ��Ӧ������������;�ʴ�Ϊ��CaO+H2O=Ca(OH)2;
������ʵ������У����۲쵽��Dװ���������ܵ�Һ�治���½���˵������ͭ�ѷ�Ӧ��ȫ��ֹͣ���ȣ�����ͨ������X����������ȴ��Ŀ���ǣ���ֹ������������ɵ�ͭ������������;�ʴ�Ϊ��Dװ���������ܵ�Һ�治���½�;��ֹ������������ɵ�ͭ������������;
�����۷���ʵ����������ݣ�����ˮ������=102.54g��102.00g=0.54g;����ͭ����Ԫ�ص�����=52.40g��51.92g=0.48g;�ɴ���֪������X��һ��û����Ԫ�أ���Ϊ0.54gˮ�к���Ԫ��0.48g;�ʴ�Ϊ��0.54;0.48;û��;
������ͨ�������Ƶ�������X�ǰ���������������ͭ�ڼ��ȵ�����������ͭ��ˮ�͵�������ƽ����;�ʴ�Ϊ��NH3;2NH3+3CuO
����3Cu+3H2O+N2;
������������������Ҫ���������������ơ��������ȡװ�ú��ռ�װ�õ�ѡ��ͬʱҲ�����˻�ѧ����ʽ����д�����˲�����ʵ��̽�����йصļ���ȣ��ۺ��ԱȽ�ǿ.�������ȡװ�õ�ѡ���뷴Ӧ���״̬�ͷ�Ӧ�������й�;������ռ�װ�õ�ѡ����������ܶȺ��ܽ����й�.���������п�����Ҫ����֮һ����Ҫ������ʵ������.

