首页> 卫生资格考试> 初级药士/药师/主管药师> 相关专业知识> 药剂学> 文章内容
2019年初级药师考试相关专业知识章节绪论之微粒分散系的主要性质与特点
来源 :中华考试网 2018-08-26
中微粒分散系的主要性质与特点
1.微粒分散体系的概念
分散体系按分散相粒子的直径大小可分为
小分子真溶液(直径<10-9m)
胶体分散体系(直径在10-9~10-7m范围):纳米微乳、脂质体、纳米粒、纳米囊、纳米胶束
粗分散体系(直径>10-7m):混悬剂、乳剂、微囊、微球
微粒分散体系具有特殊的性能:
①微粒分散体系是多相体系,分散相与分散介质之间存在着相界面,因而会出现大量的表面现象;
②随分散相微粒直径的减少,微粒比表面积显著增大,使微粒具有相对较高的表面自由能,所以它是热力学不稳定体系。因此,微粒分散体系具有容易絮凝、聚结、沉降的趋势;
③粒径更小的分散体系还具有明显的布朗运动、丁铎尔现象、电泳等性质。
2.微粒分散体系在药剂学中的意义
提高药物的溶解速度及溶解度,有利于提高难溶性药物的生物利用度;有利于提高药物微粒在分散介质中的分散性与稳定性;
大小不同的微粒分散体系在体内分布上具有一定的选择性,可以延长药物在体内的作用时间,减少剂量,降低毒副作用,还可改善药物在体内外的稳定性等。
3.微粒分散系的主要性质与特点 微粒分散体系的性质包括其热力学性质、动力学性质、光学性质和电学性质等。
(1)微粒大小与测定方法:微粒大小不均一的体系称为多分散体系。微粒分散系中常用的粒径表示方法有几何学粒径、比表面粒径、有效粒径等。这些微粒大小的测定方法有光学显微镜法、电子显微镜法、激光散射法、库尔特计数法、Stokes沉降法、吸附法等。测定纳米级粒子大小的常用方法有电子显微镜法和激光散射法。
(2)微粒大小与体内分布:
小于50nm的微粒能够穿透肝脏内皮,通过毛细血管末梢或通过淋巴传递进入骨髓组织。
0.1~3.0μm的微粒分散体系能很快被单核巨噬细胞系统的巨噬细胞所吞噬,浓集于肝脏和脾脏等部位。
7~12μm的微粒由于大部分不能通过肺的毛细血管,结果被肺部机械性地滤取。
若注射大于50μm的微粒至肠系膜动脉、门静脉、肝动脉或肾动脉,可使微粒分别被截留在肠、肝、肾等相应部位。
(3)微粒的动力学性质:布朗运动是微粒扩散的微观基础,而扩散现象又是布朗运动的宏观表现。正是由于布朗运动使很小的微粒具有了动力学的稳定性。
(4)微粒的光学性质:光的反射与散射主要取决于微粒的大小。当微粒大小适当时,光的散射现象十分明显。基于光散射的原理可以进行微粒大小的测定。
丁铎(达)尔现象正是微粒散射光的宏观表现。如果有一束光线在暗室内通过微粒分散体系,在其侧面可以观察到明显的乳光,这就是Tyndall现象。这已经成为判断纳米体系的一个简单的方法。
粗分散体系由于反射光为主,不能观察到丁铎尔现象;而低分子的真溶液则是以透射光为主,同样也观察不到乳光。
(5)微粒的电学性质:微粒的表面可因电离、吸附或摩擦等而带上电荷。
1)电泳:如果将两个电极插入微粒分散体系的溶液中,再通以电流,则分散于溶液中的微粒可向阴极或阳极移动,这种在电场作用下微粒的定向移动就是电泳。
2)微粒的双电层结构:在微粒分散体系的溶液中,微粒表面带有同种离子,通过静电引力可使与其电荷相反的离子(称为反离子)分布于微粒周围,微粒表面的离子与靠近表面的反离子构成了微粒的吸附层;同时由于扩散作用,反离子在微粒周围呈现距微粒表面越远则浓度越稀的梯度分布,从吸附层表面至反离子电荷为零处形成微粒的扩散层,吸附层与扩散层所带电荷相反。微粒的吸附层与相邻的扩散层共同构成微粒的双电层结构。
从吸附层表面至反离子电荷为零处的电位差叫动电位,即ζ电位。ζ电位与微粒的物理稳定性关系密切。ζ电位除了与介质中电解质的浓度、反离子的水化程度等有关外,也与微粒的大小有关。在相同条件下,微粒越小,ζ电位越高。
4.微粒分散体系的物理稳定性
(1)热力学稳定性:微粒分散体系是典型的多相分散体系,存在大量的相界面。热力学稳定性体现在微粒大小的改变方面。微粒越小,溶解度越大,因此在微粒分散体系的溶液中,可能出现小晶粒溶解,大晶粒长大的现象。
(2)动力学稳定性:微粒分散体系的动力学稳定性主要表现在两个方面。一个是分子热运动产生的布朗运动,一个是重力产生的沉降,二者分别提高和降低微粒分散体系的物理稳定性,当微粒较小时,布朗运动起主要作用,当微粒较大时,重力起主要作用。
粒径较大的微粒受重力作用,静置时会自然沉降,其沉降速度服从Stokes定律:
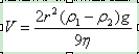
式中,V为微粒沉降速度,cm/s;r为微粒半径,cm;ρ1、ρ2分别为微粒和分散介质的密度,g/cm3;η为分散介质的黏度,P(泊)(1P=0.1Pa・s);g为重力加速度常数,cm/s2。
由Stokes公式可知沉降速度V与微粒半径r成正比,所以减小粒径是防止微粒沉降的最有效方法;同时,V与黏度η成反比,即增加介质的黏度η,可降低微粒的沉降速度;此外,降低微粒与分散介质的密度差(ρ1-ρ2)、提高微粒粒径的均匀性、防止晶型的转变、控制温度的变化等都可在一定程度上阻止微粒的沉降。沉降速度V可用来评价粗分散体系的动力学稳定性,V越小说明体系越稳定,反之不稳定。
(3)絮凝与反絮凝(*):除了热力学、动力学因素外,微粒表面的电学特性也会影响其物理稳定性。微粒表面具有扩散双电层,使微粒表面带有同种电荷,在一定条件下因相互排斥而稳定。双电层的厚度越大,则相互排斥的作用力就越大,微粒就越稳定。如在体系中加入一定量的某种电解质,可能中和微粒表面的电荷,降低双电层的厚度,降低表面所带的电量,使微粒间的斥力下降,从而使微粒的物理稳定性下降,出现絮凝状态,即微粒呈絮状,形成疏松的纤维状结构,但振摇可重新分散均匀。这种作用叫做絮凝作用,加入的电解质叫絮凝剂。
除了扩散双电层产生的斥力外,离子的强度、离子价数、离子半径等都会对微粒的带电量及双电层厚度产生影响。系统对离子选择性的吸附可以中和微粒表面的电荷而形成絮凝。
其中电解质的离子价数和浓度对絮凝的影响很大,一般离子价数越高,絮凝作用越强,如化合价为2、3价的离子,其絮凝作用分别为1价离子的大约十倍与一百倍。当絮凝剂的加入使ζ电位降至20~25mV时,形成的絮凝物疏松、不易结块,而且易于分散;增加离子浓度,降低双电层厚度,可促进絮凝;
另外,还应注意体系是否存在聚合电解质,如羧甲基纤维素、邻苯二甲酸纤维素等均带负电荷,在低浓度时具有絮凝剂的作用;若同时使用带正电荷物质会发生聚集,从而促进体系的絮凝;加入高分子物质可在微粒周围形成机械屏障或保护膜,可阻止絮凝发生;有时加入带有某种电荷的表面活性剂也可避免或减少由相反电荷造成的絮凝,如非离子表面活性剂(如吐温、司盘类等)在水溶液中常带负电荷。
如果在微粒体系中加入某种电解质使微粒表面的ζ电位升高,静电排斥力阻碍了微粒之间的碰撞聚集,这个过程称为反絮凝,加入的电解质称为反絮凝剂。如在硫酸钡的混悬剂中,当ζ电位在22mV以下时出现絮凝现象,当ζ电位在50~66mV时出现了反絮凝现象。对粒径较大的微粒体系,如果出现反絮凝,就不能形成疏松的纤维状结构,微粒之间没有支撑,沉降后易产生严重结块,不能再分散,对物理稳定性是不利的。

