2020一级结构工程师《普通化学》章节讲义:核外电子分布的规则
来源 :中华考试网 2019-11-22
中核外电子分布的规则
1)泡利不相容原理:一个原子中不可能有四个量子数完全相同的两个电子。
一个原子轨道中只能容纳自旋方向相反的两个电子。
s轨道最多容纳2电子,表示为 s2;
p轨道最多容纳6电子,表示为 p6;
d轨道最多容纳10电子,表示为 d10
2)最低能量原理:电子总是尽先占据能量最低的轨道。
电子依据近似能级图由低到高依次排布。
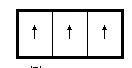
3)洪特规则:在n和ι值都相同的等价轨道中,电子总是尽可能分占各个轨道且自旋平行。
如2p3:
1.钴的价电子构型是3d74s2,钴原子外层轨道中未成对电子数是( )
A.1 ;
B. 2 ;
C. 3 ;
D. 4
答案:C
洪特规则特例:当电子的分布处于全充满、半充满或全空时,比较稳定。
全充满: p6或d10或f14
半充满: p3或d5或f7
全空: p0或d0或f0
|
。 。 。 |
结构工程师考试知多少?抢先领取资料慢慢看! |
。 。 。 | |||
| 一级结构题库 | |||||
| 加群即享 | |||||
